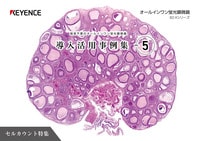
ライブセルイメージング 失敗の原因と成功のコツ
近年、ライブセルイメージング(Live Cell Imaging ※生細胞イメージング、タイムラプスイメージングとも呼ばれます)に取り組む研究者が増加しています。細胞を固定しないことにより、細胞本来の構造の変化を観察できることがメリットです。一方で、多く研究者からは、生細胞が相手であるため難易度が高く、通常の観察に比べ多くの時間を要するため、失敗に至るケースも少なくないという声を耳にします。
ここでは、ライブセルイメージングの失敗でお悩みの方や、これから取り組まれる方に向け、失敗の3大事例とその対策を紹介します。
- ライブセルイメージングの失敗例1:細胞が弱る
- ライブセルイメージングの失敗例2:ピントがずれる
- ライブセルイメージングの失敗例3:細胞が視野から逃げる
- ライブセルイメージングの実験効率を大幅に向上させる方法
ライブセルイメージングの失敗例1:細胞が弱る
ライブセルイメージングの途中や終了後、細胞の様子を確認してみると、途中で細胞が弱っていたり、細胞が死んでしまっていたり、あるいは予期せぬ状態になっていたりという現象がよく見られます。これには、いくつかの原因があります。
【原因1】光毒性が細胞にダメージを与えている
蛍光観察の際、励起光の波長が短いほど、また光が強いほど、細胞に大きなダメージを与えてしまいます。これを「光毒性※1」といい、細胞がダメージを受けて弱ったり、死んだりするだけでなく、思わぬ影響を与えることもあります。
対策
- カメラはできるだけ感度の高いものを使用する
- ゲイン※2 やビニング※3 などを併用し、弱い蛍光も感知できるように設定する
- 励起光はできるだけ弱く設定する
- 撮影設定時もなるべく励起光を当てないようする
- 撮影する枚数をできる限り少なくする
- 撮影時以外は励起光を切る
- ※1:光毒性…通常、照射する光によるダメージを指しますが、別に蛍光を発する場合、細胞が発する活性酸素によって周りの細胞がダメージを受けることも意味します。
- ※2:ゲイン…カメラが受ける電気的な信号を増幅します。増幅度を高くする(ゲインを上げる)ほど、明るく表示します。画素数は変化しませんが、ノイズが発生します。
- ※3:ビニング…仮想的に周囲の画素を結合し、単位画素あたりの受光する信号を増幅します。ゲイン増加時ほどノイズは発生しませんが、画素数が減少します。
【原因2】適切な環境が安定供給されていない
多くの細胞は、生物の体内と同等の環境を好みます。たとえば、ヒトの細胞では多くの場合、チャンバーや培養に使用するインキュベーター内の温度は37℃、二酸化炭素濃度は5%、湿度は95%以上を維持することが条件になります。この条件が安定的に供給されていないと細胞が弱ってしまい、正確なデータの取得が困難になります。
対策
- 適切な環境(温度・二酸化炭素濃度・湿度)を安定供給できるチャンバー・インキュベーターを使用する
- 室温の変化が大きい季節にはエアコンなどで室温を安定させる
- エアコンなどからの風が直接当たらないようにする
- マルチウェルプレートの端を使用する場合、水分が蒸発しないものを選択する
【原因3】菌や汚れが影響している
細胞によっては、容器に付着している菌やコンタミネーションに影響されることがあります。また、ピペットなど使用する機器もマイコプラズマ汚染※4 やクロスカルチャーコンタミネーション※5 の原因になる場合があります。
- 対策
-
- 使用する容器からピペットなどの周辺使用機器まで無菌の状態で実験する
- 細胞を持った状態では、移動を極力控える
- ※4:マイコプラズマ汚染…マイコプラズマによる感染です。細胞株が汚染される原因として、最も多い事象の1つです。
- ※5:クロスカルチャーコンタミネーション・・・扱っている細胞に別の細胞が誤って混入してしまうことです。機器を介して混入することが多いです。
- 確実なライブセルイメージングを実現する蛍光顕微鏡
- キーエンスの最新型オールインワン蛍光顕微鏡「BZ-Xシリーズ」についてカタログで詳しく見る
ライブセルイメージングの失敗例2:ピントがずれる
長時間におよぶ実験が終わり、取得したデータを確認してみると、途中からピントがずれてしまっている。この現象は、最も多い失敗事例の1つです。多くの研究者が経験している失敗ですが、原因を理解することで防止することができます。
【原因1】温度ドリフト※7 で、細胞が動く・設定が狂う
装置の電源を入れてすぐに撮影設定すると、その最中にピントがずれてしまうことがあります。原因は、電源を入れてからしばらくの間、容器内の培養液が対流し、細胞が動いてしまうためです。同時に、観察機器なども温度の変化によって多少なりとも膨張することもピントずれの原因となります。浮遊細胞・接着細胞、いずれの観察時においても設定中と撮影中のドリフトには注意が必要です。
- 対策
-
- 細胞を設置する前に、空の容器で30分間ほど暖機運転する
- 暖機運転後に細胞を置き、ピントなどの設定前にさらに30~60分ほど待つ
- ※7:温度ドリフト…温度の変化によって浮遊している細胞が動く現象や、装置自体の膨張によってピントの合う位置がずれる現象のことです。
【原因2】分裂時に細胞が動く
生きている細胞は、分裂する時、特に上下方向(Z方向)に動きます。そのため、分裂する瞬間を高倍率でワンショット撮影するとピントがずれてしまいます。
対策
- 被写界深度※8 の深い低倍レンズを使用する
- 高倍率の場合は、オートフォーカス機能またはZスタック機能を使用する
ライブセルイメージングでは、上記の予防をすることでピントのずれによる失敗を確実に防げます。この時も、励起光を当てている時間を極力短くするために、オートフォーカスやZスタックの設定範囲※9 を必要以上に大きくしないことが大切です。
- ※8:被写界深度…ピントの合う幅を表します。一般的にNAが高いほど被写界深度は浅くなります。
- ※9:Zスタックの設定範囲…Zスタックとは異なるZ位置のデータを複数枚撮影する機能です。広く細かく撮影するほど多くの情報が得られますが、その分細胞へのダメージも増加するため、極力少ない枚数で設定することが好ましいです。
- 確実なライブセルイメージングを実現する蛍光顕微鏡
- キーエンスの最新型オールインワン蛍光顕微鏡「BZ-Xシリーズ」についてカタログで詳しく見る
ライブセルイメージングの失敗例3:細胞が視野から逃げる
実験後にデータを確認してみると、途中で細胞が視野範囲外に移動してしまっている場合があります。目的の現象が完了していないうちに細胞が移動していた場合、また実験をやり直さなければなりません。
【原因】細胞が動いている
実験が長時間になるほど細胞が視野範囲から逃げてしまう可能性が高くなります。細胞が生きている以上、動くことは避けられません。さまざまな論文で細胞の細かな様子を観察したデータを目にすることがあるでしょう。それらは多くの場合、高倍率で何度も撮影を繰り返すことで得られており、多くの時間と手間を要しています。
失敗を確実に防ぐには、一度に複数箇所を撮影するか、視界を動いていく細胞に追随させながら撮影することが理想的です。
対策
- 低い倍率のレンズで視野を広く撮影する
- 一度に複数箇所を撮影する
低い倍率で視野を広く観察すれば、細胞を逃すことなく確実に捉えることができます。一方で、低倍率では細胞の細かな様子を観察できません。また、露光時間が長くなる分、撮影している間に対象が動くと画像がぶれてしまう※10 可能性もありますので注意しましょう。
- ※10:露光時間と画像のぶれ…励起光を弱くすることで、露光時間が長くなります。シャッターを開いている間に細胞が動くと、画像がぶれてしまいます。これを防ぐには。感度の高いカメラを使用することが有効です。
- 確実なライブセルイメージングを実現する蛍光顕微鏡
- キーエンスの最新型オールインワン蛍光顕微鏡「BZ-Xシリーズ」についてカタログで詳しく見る
ライブセルイメージングの実験効率を大幅に向上させる方法
これまでは、より良い研究成果を得るには、より多くの実験回数を重ね、より多くの情報を得ることが必要でした。しかし、ライブセルイメージングの場合、1回の実験に多くの時間がかかるため、何度も繰り返すには膨大な時間を要します。1回の実験でより多くの情報を取得できることが理想的です。
キーエンスのオールインワン蛍光顕微鏡「BZ-Xシリーズ」は、ライブセルイメージングの「1回の実験で得られる情報量」の問題を解消します。同時に最大999ポイントまで、2倍・4倍・20倍など、まったく異なる条件でのデータ取得が可能です。しかも、簡単に設定できるため、これまでシステムの準備と使用者の習熟にかかっていた時間も短縮します。